1. Pengertian Zat (Ing: matter)
Zat atau materi adalah sesuatu yang menempati ruang dan memiliki
massa. Menempati ruang berarti benda dapat ditempatkan dalam suatu ruang
atau wadah tertentu sedangkan massa benda dapat diukur baik dengan
perkiraan atau dengan alat tertentu seperti neraca.
Dua zat tidak dapat menempati ruang yang sama dalam waktu bersamaan. Setiap zat / materi terdiri dari partikel-partikel / molekul-molekul yang menyusun zat tersebut.
Dua zat tidak dapat menempati ruang yang sama dalam waktu bersamaan. Setiap zat / materi terdiri dari partikel-partikel / molekul-molekul yang menyusun zat tersebut.
Ilustrasi molekul-molekul penyusun zat hijau daun
2. Massa Jenis Zat (kerapatan zat; Ing: density)
 |
Zat-zat yang sejenis pasti mempunyai massa jenis yang sama. Dengan demikian dapat dikatakan bahwa massa jenis merupakan salah satu ciri khas suatu zat.
Dalam huruf Yunani massa jenis dinyatakan dalam huruf ρ (baca: rho) dan didefinisikan sebagai massa zat dibagi dengan volumenya.
Satuan dari massa jenis adalah kg/m3
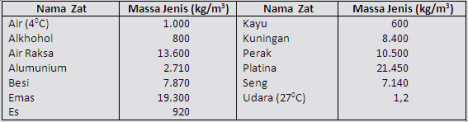
Contoh massa jenis berbagai zat.
3. Wujud Zat
Berdasarkan wujudnya zat dapat dibedakan menjadi tiga macam yaitu
padat, cair, dan gas. Masing-masing wujud zat mempunyai ciri-ciri khusus
baik dilihat dari bentuk fisiknya maupun partikel-partikel penyusunnya
sebagai berikut:
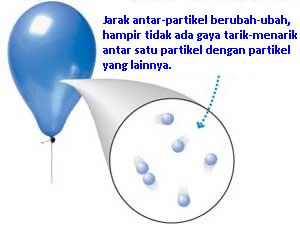
A. Zat Gas
- Letak molekulnya sangat berjauhan
- Jarak antar molekul sangat jauh bila dibandingkan dengan molekul itu sendiri.
- Molekul penyusunnya bergerak sangat bebas
- Gaya tarik menarik antar molekul hampir tidak ada
- Baik volume maupun bentuknya mudah berubah
- Dapat mengisi seluruh ruangan yang ada.
Contoh : Udara
B. Zat Cair
Contoh : air, minyak, oli
- Letak molekulnya relatif berdekatan bila dibandingkan dengan gas tetapi lebih jauh daripada zat padat.
- Gerakan molekulnya cukup bebas
- Molekul dapat berpindah tempat, tetapi tidak mudah meninggalkan kelompoknya karena masih terdapat gaya tarik menarik.
- Bentuknya mudah berubah (menyesuaikan wadah/tempatnya) tetapi volumenya tetap.

C. Zat Padat
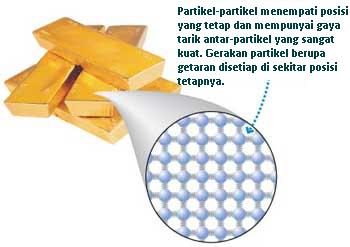
- Letak molekulnya sangat berdekatan dan teratur.
- Gaya tarik-menarik antar molekul sangat kuat sehingga gerakan molekulnya tidak bebas.
- Gerakan molekulnya terbatas, yaitu hanya bergetar dan berputar di tempat saja.
- Molekul-molekulnya sulit dipisahkan sehingga membuat bentuknya selalu tetap atau tidak berubah.
- Contoh: kayu, batu, besi
4. ADHESI DAN KOHESI
Disamping terjadi interaksi antar molekul penyusun suatu zat, maka molekul penyusun suatu zat juga dapat bereaksi dengan molekul penyusun zat yang lainnya.
Adhesi
Adhesi adalah gaya tarik menarik antara molekul-molekul zat yang tidak sejenis.
Contoh:
- Tinta dapat menempel di kertas
- Kapur / tinta dapat menempel di papan tulis
- Semen dapat melekatkan batu dengan pasir
- Cat dapat menempel pada tembok
Kohesi
Kohesi adalah adalah gaya tarik-menarik antara molekul yang sejenis.
Contoh:
- gaya tarik menarik antara molekul kayu membentuk kayu
- gaya tarik menarik antara molekuk kapur membentuk kapur batang
- gaya tarik menarik antara molekul-molekul gula membentuk butiran gula pasir
Pengaruh gaya adhesi dan kohesi terhadap zat cair menyebabkan terjadinya peristiwa –peristiwa:
A. Meniskus cembung dan meniskus cekung
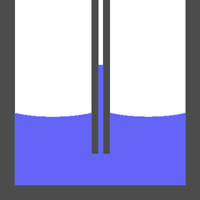
Jika adhesi lebih besar dari pada kohesi maka permukaan (meniskus)
zat cair dalam pipa kapiler cekung, misalnya pada pipa yang diisi dengan
air ( pipa kiri ). sebaliknya jika gaya kohesi lebih besar maka
permukaan zat cair dalam pipa kapiler akan cembung, misalnya pipa yang
diisi dengan air raksa ( pipa kanan).
Dalam kehidupan sehari-hari juga dapat dijumpai peristiwa adhesi dan
kohesi, misalnya ketika ada air yang jatuh di atas permukaan daun
tertentu akan membentuk bola air. Hal tersebut dikarenakan gaya kohesi
lebih besar dari adhesi.
B. Kapilaritas
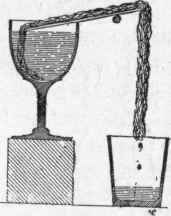
| Kapilaritas adalah
meresapnya zat cair melalui celah-celah sempit atau pipa rambut yang
disering disebut sebagai pipa kapiler. Gejala ini disebabkan karena
adanya gaya adhesi atau kohesi antara zat cair dan dinding celah
tersebut. Zat cair yang dapat membasahi dinding kaca pipa kapiler
memiliki gaya adhesi antara pipa kapiler dengan dinding pipa kapiler
lebih besar. Sedangkan zat cair yang tidak membasahi dinding kaca pipa
kapiler memilki gaya kohesi yang lebih besar. Hal ini akan mempengaruhi
tinggi rendahnya permukaan zat cair pada pipa kapiler. |
Contoh kapilaritas dalam kehidupan sehari-hari:
- Naiknya minyak tanah melalui sumbu kompor
- Naiknya minyak tanah melalui sumbu pada lampu tempel
- Baiknya air tanah sampai ke daun melalui pembuluh tapis
- Menetesnya air pada kain dalam ember yang semampai
C. Tidak berlakunya hukum bejana berhubungan.
Jika pada bejana berhubungan terdapat pipa kapiler atau terdapat
perbedaan yang signifikan dari diameter pipa-pipanya maka permukaan zat
cair dalam pipa kecil akan lebih tinggi dibandingkan permukaanya pada
pipa yang besar sehingga hukum bejana berhubungan tidak berlaku.













Tidak ada komentar:
Posting Komentar